RCH-01은 캐나다 리플리셀 제약사와
일본 화장품 기업인 시세이도와 합작하여
개발하고 있는 탈모신약이다
두 회사는 2013년에 라이센스 계약을 맺었고
리플리셀에서는 실제 2009년부터
개발하고 있었다
아래는 리플리셀 사이트에서 퍼온
RCH-01 설명이다
RCH-01 is an autologous cell therapy
utilizing dermal sheath cup (DSC) cells
isolated from the hair follicle to treat
androgenetic alopecia.
RCH-01은 모낭에서 격리된 진피피 피복컵(DSC) 세포를
활용해 안드로겐성 탈모증을 치료하는 자가세포 치료법이다.
Though several cell types are involved,
dermal sheath cup cells, located at base
of the hair follicle, regulate the growth
of hair fibres in the follicle.
여러 종류의 세포가 관련되어 있지만 모낭의 기저에 위치한
피부 껍질 컵 세포는 모낭의 성장을 조절한다.
For those people suffering from
androgenetic alopecia,
the DHT hormone attacks these cells and
as they disappear so does the hair fibre.
At the back of the head, however,
these cells are immune to the condition.
안드로겐성 탈모증을 앓고 있는 사람의 경우
DHT 호르몬은 이 세포를 공격하고 세포가 사라지면서
섬유화된다. 뒷머리쪽은 이 공격에 내성이있다.
RCH-01 is made up primarily of dermal sheath
cup cells which are immune to androgenetic
alopecia.
RCH-01은 주로 안드로겐성 탈모증에 면역된
피부 껍질 컵 세포로 구성되어 있다.
These cells are isolated from a small tissue
sample taken from the back of the
patient's scalp and used to grow
millions more of these cells which are then reintroduced into balding areas
on the subject's scalp.
이 세포들은 채취한 작은 조직 샘플로부터 격리되어 있다.
환자의 두피 뒤쪽에서부터 수백만개의 세포를 더 자라게
하곤 했는데, 이 세포들은 대상자의 두피에 있는
다발성 부위로 다시 소개된다. 두피.
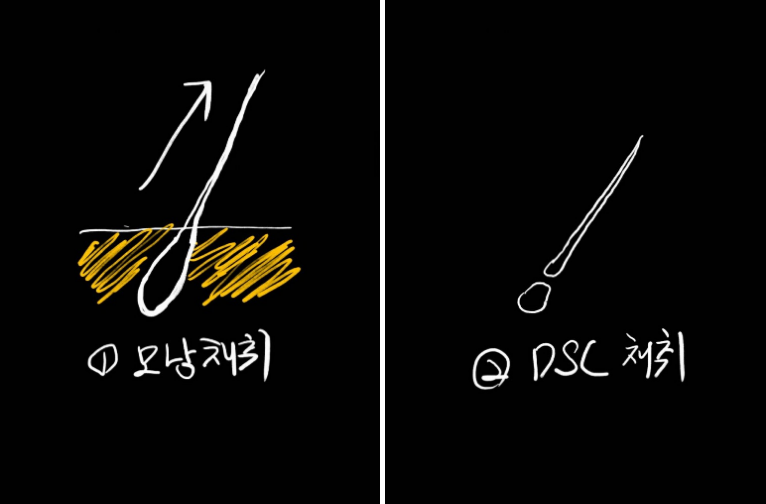
어려울게 없는 설명 쉽게 말해
DHT에 내성이 있는 뒷머리 뜯어서
배양한다음 탈모부위에 심어준다
는 말이다

유투브에 동영상도 있으니
보시면 이해하기 편하다
현재상태
In Asia, RCH-01 is being co-developed by Shiseido
Company and RepliCel. RepliCel continues
to own the rights exclusively
for the rest of the world.
아시아에서는 RCH-01이 시세이도 컴퍼니와
RepliCel에 의해 공동 개발되고 있다.
RepliCel은 세계의 나머지 지역만을 위한
권리를 계속 소유하고 있다.
Currently the product is anticipated to
launch first in Japan,
with Shiseido, while it continues
to be developed elsewhere.
Recently data was published (see below)
from a phase 2 dose-finding study
completed in Japan
demonstrating best clinical results
with the lowest tested dose.
현재 이 제품은 시세이도와 함께 일본에서
먼저 출시되는 한편,
다른 곳에서도 계속 개발될 것으로 예상된다.
최근 일본에서 완료된 2단계 선량 탐색 연구에서
가장 낮은 시험 선량으로 최상의 임상 결과를
입증하는 데이터가 발표되었다(아래 참조).
Plans are being developed for a next-phase study
to answer important questions like:
would results improve
with an even lower dose than was
tested in the phase 2 study
and how many rounds of treatments are required
to achieve optimal hair regeneration.
Trial success will be measured by assessing changesin terminal and vellus hair density
as well as cumulativehair thickness over
a period at least one year.
2단계 연구에서 테스트한 것보다 더 낮은 용량으로
결과가 개선될 수 있으며 최적의 모발 재생을 위해
얼마나 많은 치료가 필요한지와 같은 중요한 질문에 답하기 위한
다음 단계 연구를 위한 계획이 개발되고 있다.
시험 성공은 최소한 1년 동안 누적된 머리카락
두께뿐만 아니라 말단 및 벨루스 모발 밀도의
변화를 평가하여 측정될 것이다.
2단계 임상에서 좋은 임상결과를 냈다는말
2단계 임상정보
Recently RCH-01 was the subject of a clinical study
conducted at Tokyo Medical University Hospital and Toho University Ohasi Medical Center,
by Drs. Tsuboi and Niiyama.The study was
financed by Shiseido Company and each
productwas manufactured by Shiseido
at their SPEC(Cell-Processing and Expansion Center) facility in Kobe, Japan.
최근 RCH-01은 Dr.에 의해 도쿄 의대 병원과 도호 대학
오하시 메디컬 센터에서 수행된 임상 연구의 주제였다.
츠보이와 니야마. 이 연구는 시세이도 회사에서 자금을 조달했으며, 각 제품은 시세이도가 일본 고베에 있는
세포처리및 팽창 센터(SPEC) 시설에서 제조했다.
RepliCel helped Shiseido design, validate,
and prepare the SPEC facility for certification
by Japan’s PMDA
(Pharmaceuticals and Medical Device Agency).
Shiseido’s SPEC team was also trained by
RepliCel and Innovacell in the GMP (Good Manufacturing Practice)
compliant production protocols for RCH-01.
ReplicCel은 Shiseido가 일본 PMA
(Pharmacy and Medical Device Agency)의
인증을 위한 SPEC 시설을 설계, 검증 및 준비하는 데
도움을 주었습니다.
Shiseido의 SPEC 팀은 RCH-01을 위한 GMP
(Good Manufacturing Practice)
호환 생산 프로토콜에서 ReplicCel과 Innovacell로부터도 교육을 받았습니다.
The study data from this randomized,
placebo-controlled, double-blinded,
dose-ranging clinical study of 65 patients
(male and female) with pattern hair loss confirms,
with statistical significance, the observations from RepliCel’s phase 1 trial in a larger cohort of patients including females, a wide variety of
ages and hair loss, and compared with
a placebo-control. In summary, the study produced a statistically significant and clinically meaningful increasein hair density and
diameter as measured
nine months after treatment. See .
65명의 환자(남성 및 여성)와 패턴 탈모에 대한 무작위적이고
위약 제어, 이중 블라인드, 선량 범위 임상 연구의
연구 데이터는 통계적으로 유의미하게 ReplicCel의 1단계 임상 실험의 관찰을 여성, 다양한 연령 및 탈모 환자
코호트에서 확인하며 비교한다.플라시보 조절을 하다 요약하자면, 이 연구는 치료 후 9개월 후에
측정된 머리 밀도와 지름을 통계적으로 유의미하고
임상적으로 의미 있는 증가를 보여 주었다. 보다
”Autologous Cell-based Therapy for Male and Female Pattern Hair Loss using Dermal Sheath
Cup Cells: A Randomized Placebo-Controlled Double-Blinded Dose Finding Clinical Study”. American Academy of Dermatology.
"피부 피복 컵 세포를 이용한 남성 및 여성 패턴 탈모에 대한
자가 세포 기반 치료: 무작위 플라시보 조절
이중 블라인드 선량 발견 임상 연구" 미국 피부과학원
https://doi.org/10.1016/j.jaad.2020.02.033
Redirecting
linkinghub.elsevier.com
65명 환자대상 임상에서 밀도와 지름에서
유의미한 결과를 얻었고
미국 피부과학원에 실었다는말
임상실험 결과
Background
Few effective treatments are available for male pattern hair loss
(MPHL) or, especially, for female pattern hair loss (FPHL).
Recently, cell-based therapies using autologous
or allogeneic cells have been used clinically.
Objective
We examined the safety and efficacy of autologous
cell–based therapy using dermal sheath cup
(DSC) cells to treat MPHL and FPHL.
Methods
DSCs dissected from occipital hair follicles were
cultured to manufacture DSC cells. Participants with MPHL
or FPHL received single injections of 7.5 × 10 6, 1.5 × 10 6, or 3.0 × 10 5
DSC cells or a placebo in 4 randomized separate
regions on the scalp, and hair densities and diameters
were measured for 3, 6, 9, and 12 months.
Results
Fifty men and 15 women aged 33 to 64 years were
injected with DSC cells. Total hair density and cumulative hair
diameter at the 3.0 × 10 5 DSC cells injection site was significantly
increased compared with the placebo after 6 and 9 months
. Men and women showed similar improvements,
and there were no serious adverse events.
Limitations
No lower cell numbers were tested, and the
positive effect was temporary until 9 months.
Conclusion
The results suggest that cell therapy with autologous DSC cells
may be useful as a new therapeutic method for treating MPHL and FPHL.
배경
남성 패턴 탈모(MPHL) 또는 특히 여성 패턴 탈모(FPHL)에
대한 효과적인 치료법은 거의 없다. 최근, 자가 또는 이질 세포를 이용한 세포 기반 치료법이 임상적으로 사용되고 있다.
목적
우리는 MPHL과 FPHL을 치료하기 위해 피부피복(DSC) 세포를 이용한 자가 세포 기반 치료법의 안전성과
유효성을 조사했다.
방법들
후두 모낭에서 해부된 DSC는 DSC 세포를 제조하기 위해 배양되었다.
MPHL 또는 FPHL을 사용하는 참가자들은 두피에
7.5 × 106, 1.5 × 106 또는 3.0 × 105 DSC 세포 또는
위약을 한 번 주입받았고, 머리카락 밀도와 지름은
3, 6, 9, 12개월 동안 측정되었다.
결과.
33세에서 64세 사이의 남자 50명과 여자 15명이 기무사 세포를
주입받았다. 3.0 × 105 DSC 세포 주입 부위의 총 머리카락 밀도 및 누적 머리카락 직경은 6개월 및 9개월 후 위약에
비해 크게 증가했다. 남자와 여자는 비슷한 향상을 보였고, 심각한 부작용은 없었다.
한계
더 낮은 셀 수는 검사되지 않았으며, 양성 효과는
9개월까지 일시적으로 나타났습니다.
결론
결과는 자가 DSC 세포를 이용한 세포 치료가 MPHL과 FPHL을 치료하는 새로운 치료 방법으로 유용할
수 있다는 것을 암시한다.
65명 환자대상 임상에서 밀도와 지름이
위약을 받은 사람에 비해 크게 증가했다
1번 받았을때 효과는 9개월까지
2009년부터 개발을 시작한 RCH-01은
아직 임상중
위 내용들은 2020년 3월 23일에 발표한내용이다
밀도와 굵기가 얼만큼 증가했는지에 대해서
구체적인 내용이 없어 아쉽다
이론적으로는 DHT에 내성이 있는 뒷머리를 뜯어
배양한다음 탈모부위에 넣어주는건데
이론적으로는 더할나위없다
자가모발이식의 경우
생착률을 생각하면 실질적으로
전체적인 숱은 마이너스가 된다
RCH-01은
내 모낭을 자가복제 하는것이어서
뒷머리 숱이 줄어드는것도 아니고
마이너스는 없는데 플러스는 있으니까
허나
정말 쉽지 않나보다
모낭을 추출하는 기술
모낭에서 DSC를 분리하는기술
DSC를 배양하는 기술
DSC를 다시 두피에 넣어주는기술 등
언제 상용화될지는 모른다
되어도 합작회사인 일본부터 시행된다
우리나라는 한 2~3년정도 늦게 들어오겠지
만약 들어와도 저 기술력 정도면
대학병원에서 전문팀이 꾸려져야 하지 않을까
일반 피부과 의원에서는 감당 못할것 같다
당연히 가격도 높을것이다
한대 맞는데 100만원정도라고 얼핏들은것 같기는
한데~ 한번 맞고 9개월 지속되면
탈모인에게는 남는 장사다
부작용도 없기때문에
언제출시될지 모르기때문에
탈모약 먹고 존버하시길 빈다
'탈모신약' 카테고리의 다른 글
| PRP(자가혈소판 풍부 혈장 치료술) 탈모치료 (0) | 2021.01.24 |
|---|---|
| 엑소좀과 탈모치료 (0) | 2021.01.24 |
| Setipiprant(세티피프란트) 탈모신약 가능성 (0) | 2021.01.24 |
| Fevipiprant(페비비프란트) 탈모신약 분석 (0) | 2021.01.24 |
| RU58841(PSK3841)은 탈모신약 가능성 (0) | 2021.01.24 |




댓글